Efecto del Dobesilato Cálcico en la progresión de la Retinopatía Diabética temprana:
un estudio doble ciego aleatorio
María L. Ribeiro, Andras I. Seres, Angela M. Carneiro, Michael Stur, Alain Zourdani, Patricia Caillon, José G. Cunha-Vaz, en representación del Grupo de Estudio de Doxium-Retinopatía
*Recibido: 12 setiembre 2005; Revisado: 21 febrero 2006; Aceptado: 23 febrero 2006
Resumen
Antecedentes: Estudio para confirmar el efecto del dobesilato cálcico (CaD) comparado con placebo (PLA) sobre la permeabilidad de la barrera hemorretiniana (BHR) en la retinopatía diabética temprana (RD). Métodos: Se incluyeron en este estudio doble ciego controlado con placebo, adultos con diabetes tipo II y retinopatía diabética temprana (< nivel 47 Clasificación ETDRS) y PVPR entre 20 y 50x10-6/min). El tratamiento fue de 2 g/día de CaD por 24 meses. El parámetro primario, PVPR, fue medido cada 6 meses con fluorofotometría. Los parámetros secundarios fueron las fotografías de fondo de ojo, la angiografía con fluoresceína y la evaluación de seguridad. El control metabólico se hizo cada 3 meses. Resultados: 194 pacientes comenzaron el estudio (98 CaD, 96 PLA), 137 lo completaron a los 24 meses (69 CaD, 68 PLA). Ambos grupos de tratamiento fueron comparables al inicio del estudio, con ETDRS nivel 10 en 59% de los pacientes. El cambio promedio en valores del PVPR, desde el inicio del estudio hasta después de los 24 meses, fue significativamente menor (P=0.002) en el grupo CaD [-3.87 (SD 12.03)] que en el grupo PLA [+ 2.03 (SD 12.86)], correspondiendo a una reducción de 13.2% en el grupo CaD y a un incremento de 7.3% en el grupo PLA. La evolución del PVPR fue analizada también según las clases de HbA1c (<7%, entre 7 y 9%, ?9%) y los resultados confirman la superioridad del CaD independientemente del nivel de control de diabetes. También se obtuvo una alta diferencia significativa [CaD: -3.38 (SD 13.44) contra PLA: +3.50 (SD 13.70)] en un subgrupo de pacientes sin tratamiento antihipertensivo y/o hipolipemiante (P=0.002 a los 24 meses). Un análisis de los parámetros secundarios mostró cambios significativos a favor del CaD desde el inicio del estudio hasta la última visita en la progresión de las hemorragias (P=0.029), nivel de RD (P=0.0006) y microaneurismas (P=0.013). Seguridad:Solo el 2.5% de todos los eventos adversos reportados fueron evaluados como probablemente relacionados con la droga, y todos los eventos adversos serios fueron reportados como improbables. Conclusión: 2 g de dobesilato cálcico al día por 2 años muestran una actividad significativamente mejor que placebo en la prevención de la disrupción de la BHR, independientemente del control de diabetes. La tolerancia fue muy buena.
Palabras clave: Retinopatía diabética, barrera hemorretiniana, coeficiente de penetración del vítreo posterior, dobesilato cálcico.
Introducción
La diabetes mellitus tipo 2 es una enfermedad crónica frecuente y costosa y con creciente prevalencia (34,47,49). Una complicación es la retinopatía diabética (RD), que causa compromiso visual y ceguera(7) cuya progresión puede ser retrasada con adecuado control de la glicemia (37), lo que es difícil en la práctica. La fotocoagulación con láser puede prevenir la pérdida visual, sin embargo puede alterar la calidad de vida del paciente, pues puede causar pérdida de visión nocturna periférica (36,41) o empeoramiento (1). Es mejor un tratamiento farmacológico en las primeras etapas de la RD que disminuya su progresión. Se han sugerido aspirina (2,15), inhibidores ECA (9,38), antagonistas de receptores de angiotensina I y II (10,23,29,45) e inhibidores de la isoforma beta de la proteín-quinasa C (19), cuyos beneficios terapéuticos deben aún ser demostrados. El dobesilato cálcico (CaD) es un compuesto sintético efectivo en trastornos microcirculatorios (20,25,30,44) y que ha demostrado que reduce la progresión de la RD (3,4,20,42) y el escape de proteínas, y mejora la angiografía con fluoresceína y fotografía del fondo de ojo (42). El PVPR fue el objetivo primario de un estudio piloto previo, a que a dosis de 2 g/dia por 12 meses estabilizó la permeabilidad de la BHR (30). Este estudio quiere confirmar la eficacia de CaD para restaurar la BHR en una gran población de pacientes a la dosis oral de 2 g/dia por 2 años.
Materiales y métodos
Pacientes
Se incluyó sujetos de ambos sexos, entre 40 a 75 años, con diabetes tipo 2 estable, retinopatía mínima (< nivel 47 escala Wisconsin) (16) y PVPR entre 20 y 50x10-6/min, (VN = 15.9+4.7x10-6/min) (12). Los criterios de exclusión fueron: edema macular, enfermedades vasculares de la retina o sinéresis vítrea y terapia previa con láser. Este estudio aleatorio doble ciego controlado con placebo fue realizado en 8 centros europeos, con aprobación de los comités de ética, autoridades nacionales, y consentimiento escrito de los pacientes.
Tratamiento
Los pacientes fueron asignados aleatoriamente al tratamiento activo dos cápsulas de CaD de 500 mg ó a placebo (PLA), administrados dos veces al día, por 24 meses, el cumplimiento se evaluó mensualmente y se monitoreó el cumplimiento de las buenas prácticas clínicas.
Evaluación clínica
El objetivo primario de eficacia fue el cambio en el PVPR durante todo el estudio, a los 24 meses y en la última visita disponible, medido cada 6 meses. Los exámenes fueron tomados antes de la administración intravenosa de fluoresceína (14mg/kg) y 60 minutos después de 10, 15 y 50 minutos para medir la concentración de fluoresceína en el plasma (11,30). Objetivos secundarios de eficacia fueron la evaluación de retina con fotografía del fondo de ojo (graduación de Wisconsin) (16,28) y evaluaciones angiográficas (calificación ETDRS) (17), cada 6 meses. También se evaluó agudeza visual, presión intraocular, los eventos adversos cada 3 meses, y glicemia en ayunas y HbA1c.
Métodos Estadísticos
Todos los pacientes que recibieron al menos una dosis de la medicación del estudio fueron incluídos en el análisis de seguridad. La eficacia fue analizada para la población por intención de tratar (ITT) (todos los pacientes que ingresaron a la fase de tratamiento con al menos una medida de eficacia después del inicio del estudio). El peor ojo de cada paciente, evaluado con PVPR y con fotografía del fondo de ojo, fue usado para el análisis de eficacia primario. Se realizó un análisis más profundo de los parámetros secundarios para investigar si la elección del peor ojo basado en los niveles PVPR introdujo un sesgo que impidiera el descubrimiento de una diferencia entre CaD y PLA en los resultados de la retinografía estereoscópica. Este análisis estuvo basado en el "peor" fondo de ojo en vez del ojo con el "peor" PVPR del análisis previo. El "peor" fondo de ojo para cada paciente fue definido como el ojo con más alto valor del nivel de RD al inicio del estudio. Se investigaron los siguientes parámetros en el fondo de ojo:hemorragias, microaneurismas y nivel de RD. La comparación entre ambos grupos fue llevada a cabo al inicio del estudio para verificar su homogeneidad en relación a las variables demográficas usando pruebas de significancia de dos lados. El análisis de eficacia fue realizado con ANCOVA. Las diferencias de los valores de PVPR a los 24 meses y en la última visita disponible comparados con los valores PVPR iniciales, fueron comparados con la prueba de Mann-Whitney y con la prueba de Wilcoxon. Un análisis de subgrupo fue realizado mientras los datos estuvieron en ciego de acuerdo a los niveles promedio de HbA1c. LOs parámetros de eficacia secundarios fueron comparados con la prueba de Mann-Whitney. Las variables de seguridad (eventos adversos y valores de laboratorio) fueron comparados usando la prueba exacta de Fisher o la prueba de Mann-Whitney. Para el cálculo del tamaño de muestra, la diferencia en el coeficiente de penetración entre CaD Y PLA fue asumida como de 3.4x10-6/min (ajustado a partir de 0.6, como fue reportado en el estudio piloto) (30). Debido a la alta incidencia de abandonos en un estudio de 24 meses con pacientes ambulatorios, se calculó que eran necesarios 240 pacientes para proveer aproximadamente 130 casos analizables. Los cálculos estadísticos fueron concluidos usando NCSS versión 2004 (NCSS, Kaysville, EEUU), Systat V. 9.0 (SPSS Inc. Chicago, III., EEUU) y Testimate v.5.02 (IDV, Gauting, Alemania).
Resultados
Pacientes
De los 299 pacientes sometidos a revisión, 197 fueron elegibles para la aleatorización después de la primera visita de selección, 194 comenzaron tratamiento (98 CaD, 96 PLA), quienes formaron la población de seguridad. La población de eficacia (población ITT) comprendió a los 169 pacientes (87 CaD, 82 PLA) que acudieron a la primera visita de eficacia en el mes 6. El estudio fue completado por 137 pacientes (69 CaD, 68 PLA). La razón principal para la descontinuación del estudio fue la aparición de un evento adverso (nueve de los tratados con CaD, ocho de los que recibieron PLA) o sus consecuencias (ejemplo uso de medicamentos no autorizados). Las características demográficas y valores iniciales de los dos grupos fueron similares. El nivel de la RD en el inicio del estudio fue similar en ambos grupos, con nivel 10 en 59.3% en el grupo CaD y 58.5% en el grupo PLA. La duración promedio del tratamiento fue de 676.5 días (SD 136.5) para el grupo CaD y 679.4 días (SD 131.8) para el grupo PLA. El cumplimiento fue de 95% para ambos grupos.
Eficacia
El cambio en el PVPR fue significativamente mejor en el grupo de tratamiento activo comparando los valores al inicio del estudio con los de la última visita disponible (P=0.006) y con los valores a los 24 meses (P=0,002) con respecto a PLA (Fig.2). El PVPR decreció desde el inicio del estudio hasta los 24 meses en el grupo de tratamiento activo [-3.87 (SD 12.03) 10-6/min que corresponde a un porcentaje de disminución de 13.2% contra el inicio del estudio (P<0.001)]. En el grupo placebo, el PVPR se incrementó en 7.3% en 24v meses.
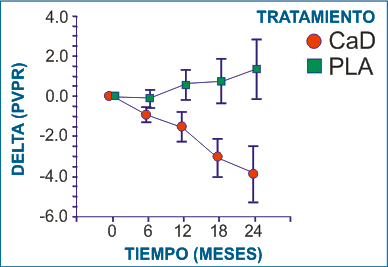 |
| Figura 2. Progresión de PVRP (media±ESM) durante el estudio, P=0.002 al mes 24; datos obtenidos por regresión robusta. CaD: dobesilato cálcico; PLA: placebo. |
En los valores del PVPR desde el inicio del estudio hasta la última visita disponible, se observó disminución significativa en el grupo de tratamiento activo de -12.4% y un incremento no significativo en el grupo placebo de 4.5%. (Fig.3). Desde el inicio del estudio el PVPR decreció significativamente en más pacientes en el grupo de tratamiento activo (61 pacientes mejoraron, 25 no) en comparación con el grupo de placebo (43 pacientes mejoraron, 39 no) en la última visita (P=0.018). En el análisis de regresión múltiple las únicas variables que correlacionan significativamente con el cambio en el PVPR desde el inicio del estudio, fueron el PVPR en el inicio del estudio (a favor del tratamiento activo; P<0.001) y el tratamiento (a favor de la progresión más lenta;P=0.002).
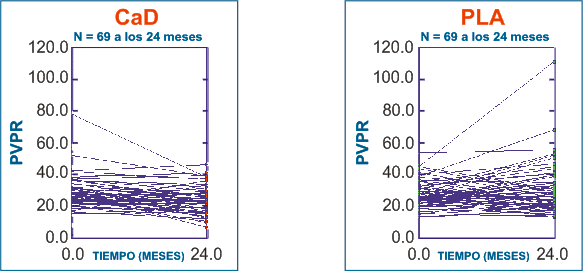 |
| Figura 3. Evoluciones individuales del PVPR desde el inicio del tratamiemto hasta 24 meses. CaD: dobesilato cálcico; PLA: placebo; n: número de pacientes. |
En el análisis de subgrupo con respecto al control de la diabetes, el PVPR en el grupo tratado con CaD mejoró significativamente en 24 meses para los pacientes con HbA1c<7% (P=0.043) y entre 7 y 9% (P=0.05), y sobre el total del periodo del estudio (P=0.044) (21) para pacientes con HbA1c > 9% (Fig. 4). En relación a la medicación concominante, 33 pacientes del grupo de tratamiento activo y del grupo PLA la recibieron antihipertensivos y/o agentes hipolipemiantes aparte del tratamiento para la diabetes. La figura 5 muestra los efectos del tratamiento en la progresión del PVPR de acuerdo a si el paciente tomó estos agentes o no. Se confirmó que la evolución del PVPR desde el inicio del tratamiento hasta los 24 meses en el grupo activo fue en el grupo activo fue significativa en la presencia de estas drogas (P=0.011), lo que no fue el caso en el grupo PLA (P=0.223).
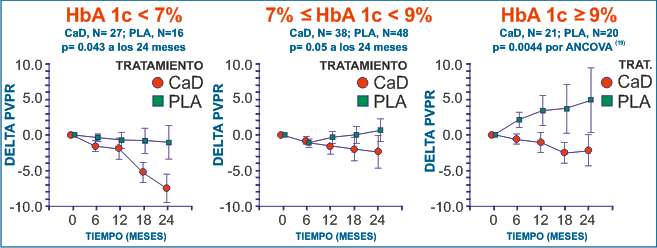 |
| Figura 4. Evolucion del PVPR (media±ESM) según el nivel del HbA 1c (datos obtenidos por regresión robusta) desde el inicio del tratamiemto hasta 24 meses. CaD: dobesilato cálcico; PLA: placebo; n: número de pacientes al inicio del estudio. |
En los pacientes sin estos medicamentos, el PVR mejoró significativamente a los 24 meses en el grupo CaD (P=0.002) en comparación con el grupo placebo [CaD: -3.38 (SD 13.44) versus PLA: + 3.50 (SD 13.70)].
Con relación a la progresión de las hemorragias desde el inicio del estudio hasta la última visita fue significativamente en favor de CaD en comparación a PLA (P=0.029) (Figura6). El número de hemorragias decreció significativamente en más pacientes en el grupo de tratamiento activo en comparación al grupo de placebo en la última visita (P=0.036). La evolución del conteo de microaneurismas desde el inicio del tratamiento hasta la última visita mostró una tendencia a favor del grupo CaD (P=0.066).
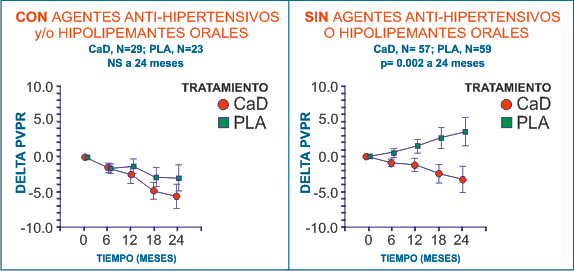 |
| Figura 5. Progresión del PVPR (media±ESM) según la administración de tratamientos concomitantes. CaD: dobesilato cálcico; PLA: placebo; n: número de pacientes al inicio; NS: no significarivo. |
Clasificando los microaneurismas por clases (18) la diferente progresión es evidentemente positiva a favor de CaD. Finalmente, la evolución de RD desde el inicio del estudio hasta la última visita muestra una diferencia altamente significativa a favor de CaD (P<0.001) (Fig. 6). El análisis de los parámetros del fondo de ojo, considerando el peor ojo basado en el nivel de RD, confirma la diferencia significativa a favor de CaD para las hemorragias, microaneurismas y nivel de RD.
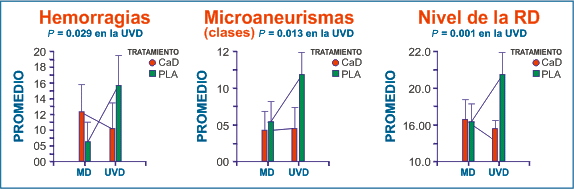 |
| Figura 6. Evolución de los parámetros del fondo de ojo desde el inicio del estudio hasta la última visita. CaD: dobesilato cálcico; PLA: placebo; UVD: última visita disponible. |
Seguridad
De los 194 pacientes (98 CaD, 96 PLA) que forman la población de seguridad, 93 (49 CaD, 44 PLA) presentaron quejas de 202 eventos adversos (115 CaD, 87 PLA), pero solo 5 (tres CaD, dos PLA) fueron catalogados por los investigadores como probable o posiblemente relacionados con la droga. Todos los eventos adversos serios con la droga en estudio fueron reportados como “improbables” (21 CaD, 18 PLA).
Discusión
El escape vascular es el primer proceso en la fisiopatología de la RD (31,32), y puede ser el inicio de eventos que pueden conducir a una eventual ceguera. El escape de fluoresceína hacia el vítreo es un indicador potencial de pronóstico de consecuencias finales relevantes como la perdida visual debida a edema macula o la necesidad de fotocoagulación (8, 13, 50). Recientemente se ha descubierto que el dobesilato cálcico actúa en los mecanismos bioquímicos básicos involucrados en la retinopatía diabética. Resultados in vitro e in vivo sugieren que el CaD posee propiedades antioxidantes a través de un efecto barrendero de las radicales libres (5,6,60). CaD reduce considerablemente los niveles AGEs (productos finales de glicación avanzada) y VEGF (factor de crecimiento de endotelio vascular) en la retina y revierte la hipermeabilidad de la retina en ratas diabéticas con retinopatía preproliferativa (40,48) reduciendo la formación de productos de glicación avanzada de carboximetil-lisina (CML-AGE) a través de sus propiedades antioxidantes y que estos a su vez disminuyen la sobre expresión de VEGF y los escapes secundarios de albúmina. Las evidencias farmacológicas previas sugieren que el CaD puede estabilizar la barrera hemorretiniana en pacientes con retinopatía diabética mediante un mecanismo antioxidante (22). Varios estudios clínicos doble ciego controlados con placebo demostraron la eficacia de CaD en la disminución de la progresión de la RD. La mayoría de ellos fueron llevados a cabo con pequeñas cohortes, bajas dosis y estudios de corta duración y sus parámetros de evaluación estuvieron únicamente basados en angiografías con fluoresceína o fotografías del fondo de ojo, pero ninguno evaluó el PVPR. En los 90s, un estudio controlado contra no tratamiento (26), con dosis de 1.5 g CaD/día y con un seguimiento de 2 años, no mostró reducción en la progresión de la RD, pero el consumo de la droga en este estudio fue mal controlado, con lo cual explicaron la falta de eficacia. Por otro lado, un estudio piloto doble ciego controlado con placebo con 47 pacientes (30) reporto que el PVPR permanece estable en pacientes con RD temprana que recibieron CaD 2 g/día por 12 meses. Como en el estudio piloto, aquí estudiamos los efectos del CaD sobre el PVPR en pacientes con RD inicial, pero en 2 años y en una más amplia cantidad de pacientes. Este estudio mostro un significativo mejoramiento progresivo en el PVPR con respecto al inicio del estudio en el grupo tratado con dobesilato cálcico durante 24 meses del estudio (p<0.0001). El grupo placebo, de otro lado, no mostró cambios significativos con respecto al inicio del estudio. La comparación directa del tratamiento con CaD con PLA mostró un efecto significativo del tratamiento activo (P=0.006 para el cambio desde el inicio del estudio hasta el último valor disponible, P=0.002 para el cambio desde el inicio de estudio hasta el valor de 24 meses). Como se esperaba en una población con RD mínima, el tratamiento con CaD no influencio en la agudeza visual ni en la presión intraocular. Sin embargo, los parámetros del fondo de ojo mostraron diferencias significativas a favor del CaD en la evolución de las hemorragias, los microaneurimas y los niveles de RD, cuando se tomo en consideración el peor ojo basado en el nivel de RD al ingresar al estudio. Debido a que los elevados niveles de hemoglobina glicosilada se correlacionaron con un rápido índice de progresión de la RD (33,43), analizamos la progresión del PVPR mediante el grado del control metabólico. En este análisis, el control del escape a través de la BHR fue significativamente menor en el grupo tratado con CaD que en el grupo de PLA, sin tener en cuenta el grado de control metabólico. En la última visita, la evolución de los parámetros del fondo de ojo en relación al subgrado de HbA1c, también dieron diferencias significativas a favor del grupo que recibió CaD, principalmente para los pacientes con HbA1c>9%, hipertensión (35,39) e hipercolesterolemia también se correlacionan con el mal pronóstico de la RD, pudiendo prevenirse con antihipertensivos e hipolopemiantes. También se investigo la posible influencia de los agentes antihipertensivo y/o de los agentes hipolipemiantes sobre el resultado principal del presente estudio. Casi el 40% de nuestra población ITT estuvo tomando al menos uno de estos agentes, y su uso parece reducir el cociente del PVPR tanto en el grupo de CaD como en el grupo PLA. Concluimos que el CaD disminuye significativamente la permeabilidad de la BHR medida con el valor del control metabólico o del uso de antihipertensivos y/o hipolipemiantes. CaD tuvo un efecto significativamente beneficioso en el control de hemorragias y la progresión global de la RD. Nuestras conclusiones sugieren que el CaD puede disminuir la progresión del escape en la RD. Estos datos podrían ser base para diseñar estudios sobre la eficacia de CaD sobre el pronóstico de la agudeza visual y la necesidad de fotocoagulación en el edema macular.
Información proporcionada por OM PHARMA.
Graefe’ Arch Clin Exp Opthalmol.
DOI 10.1007/s 00417-006-03 18-2 |
