”¿Adónde va la Medicina? Reflexiones sobre la Medicina del Futuro”
Javier Arias-Stella (1)
Vivimos una etapa sorprendente en la evolución de la Medicina. Los avances tecnológicos y científicos van más rápido que nuestra imaginación y capacidad de asimilarlos.
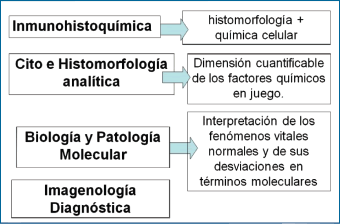 |
Gráfico 1.
|
Y todos nos preguntamos ¿adónde nos conducen estos avances? ¿Y cuándo y en qué tiempo culminará la obtención de las metas perseguidas? (1-4) (Gráficos 1, 2 y 3).
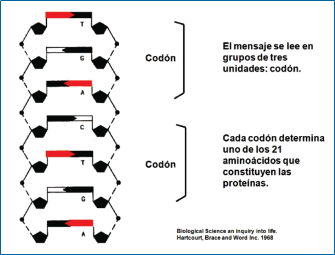 |
Gráfico 2.
|
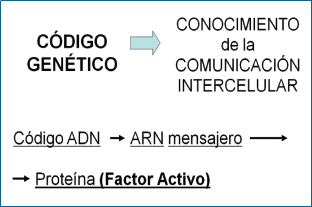
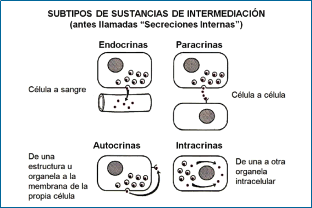
Con el develamiento de la estructura del ADN (Gráficos 4, 5 y 6), la ciencia médica logró recién entender el lenguaje celular y la relación con factores transcriptores y sustancias de intermediación como nunca antes ocurrió en la historia de la medicina (6-9).
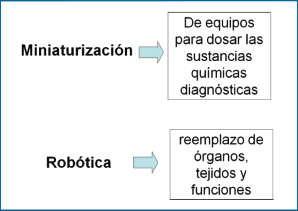 |
Gráfico 3.
|
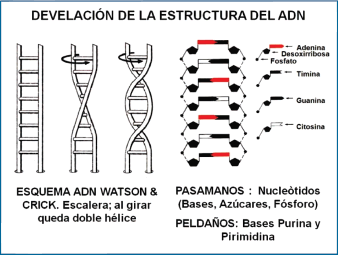 |
Gráfico 4.
|
Todo indica que -en pocos años- estaremos delante de una nueva forma de acción y enfoque de lo que hemos concebido, hasta hoy, como el ejercicio correcto de la medicina.
Esta es la impresión de todos los expertos y la conclusión de las conferencias que se han realizado y se hacen sobre el tema.
Para citar solo una de ellas, el Dr. J.N. Schwartz, Presidente del Colegio Americano de Patología, después de recorrer, durante los últimos dos años, universidades e institutos académicos discutiendo ese horizonte, concluyó hace poco: “todos hablan de los cambios dramáticos que enrumban a una transformación en el ejercicio, docencia y metas de la medicina” (5).
 |
| Gráfico 5 |
 |
| Gráfico 6 |
El asunto es que estos cambios vienen ocurriendo con una rapidez que se incrementa con el tiempo y que lo que veíamos hace algunos años o meses recientes: Nanomedicina-Nanoterapéutica, Epigenética y nueva Biología Molecular, Miniaturización de equipos para dosar la sustancias químicas diagnosticas, Robótica y reemplazo de órganos y funciones; como una cosa del futuro, son ya materias que están estudiándose no solo en el laboratorio experimental, sino ensayándose, en sus fases iniciales, en la clínica; y que los optimistas consideran que será una realidad rutinaria en menos de 10 ó 15 años.
En una u otra forma todos los aquí presentes hacen hoy, de manera puntual y para casos singulares, uso de estas tecnologías que se vienen introduciendo progresivamente en todas las especialidades.
El llamado “Modelo de Salud Temprana”
Con este panorama y esta amplitud de nuevos factores en juego es difícil intentar una discusión ordenada de las fuerzas que hoy intervienen en este cambio. Necesariamente tenemos que ser arbitrarios en la escogencia de los temas a discutir, por las limitaciones de tiempo y respeto a la paciencia de los oyentes. Hay también que ser acertado en esta
escogencia y tener capacidad de síntesis. No estoy dotado de esos talentos y por lo tanto lo que diga deberá tomarse con la reserva que esas consideraciones subrayan.
Se me ocurre abrir estos comentarios refiriéndome a lo que se ha venido en llamar “The Early Health Model”, el “Modelo de Salud Temprana”. Puesto en pocas palabras su definición es: “Diagnóstico en la etapa pre-sintomática y pre-clínica de la enfermedad” (10). Esto es, descubrir la inminencia de la enfermedad antes de que ella se establezca. Nos motiva hoy la posibilidad de inventar pruebas y equipos que nos permitan reconocer la etapa previa o potencial para que se desarrolle una enfermedad antes que esta se haya manifestado. Esto es, averiguación en el hombre sano de su potencial para desarrollar un mal.
Con este objetivo compañías y empresarios, viendo las ganancias futuras de sus inversiones -tales como General Electric (Fairfield, Conn.) y Siemens Medical Solutions USA (Malvern, Paterson.)- están embarcados en el desarrollo de noveles equipos y pruebas.
Los grandes centros donde se están actualmente haciendo ensayos clínicos en esta dirección son:
• Instituto Tecnológico de California
• Instituto de Sistemas Biológicos de Seattle
• Escuela de Medicina de Johns Hopkins
• Escuela de Medicina de Harvard
• Babraham Institute de Cambridge
• Columbia University
• Escuela de Medicina de Emory
• Rockefeller University
•Memorial Sloan-Kettering Cancer Center
(Gráfico7),
 |
| Gráfico 7 |
y algunos de los investigadores
principales implicados son:
• James R. Heath
• Mark E. Davis
• Leroy Hood
• Stephen Baylin
• Wolf Reik
• J. Craig Venter
• George Church
(Gráfico 8).
 |
| Gráfico 8 |
El Concepto de Red Malla
Orgánica Interconectada
Los investigadores del Instituto Tecnológico de California consideran los órganos, tejidos y células que componen el ser humano como un sistema de redes interconectadas (Gráfico 9). Los círculos blancos sólidos son proteínas que interactúan unas con otras (líneas blancas), cada una de estas proteínas tiene, en condiciones de normalidad, un nivel cuantificable (11).
 |
Gráfico 9
|
Para modelar un sistema se requiere una vasta cantidad de datos y los organismos vivos están llenos de información que se puede describir como digital -ella puede ser medida y cuantificada en un modelo. Esta información biológica comienza con el código genético de un organismo (Gráfico 10). Cada célula en el cuerpo humano lleva consigo una copia completa del genoma humano que está compuesto de tres mil millones de pares de bases de ADN, las letras del alfabeto genético.
 |
| Gráfico 10 |
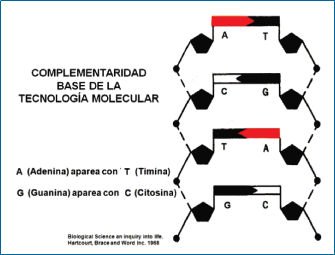
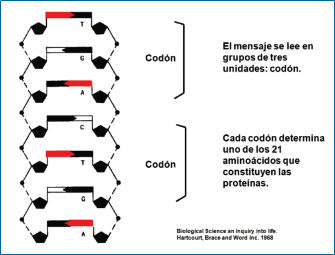
Estas letras codifican 25,000 genes que representan instrucciones específicas para el desarrollo y funcionamiento de las células y tejidos. Dentro de cada célula los genes son
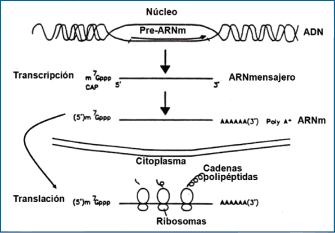
transcriptos a una forma más viable (Gráficos 11, 12 y 13), pedazos menores de ARN mensajero que llevan estas instrucciones a un equipo celular que lee el ARN y elabora cadenas de aminoácidos según las instrucciones del código (6). Luego, las cadenas de aminoácidos formados se acomodan para constituir polipéptidos y proteínas, las máquinas tridimensionales moleculares que ejecutan las funciones de la vida. .
 |
| Gráfico 11 |
 |
| Gráfico 12 |
 |
| Gráfico 13 |
Dentro de un sistema biológico tal como una persona (Gráfico 14), toda esta “data” se trasmite, procesa, integra y finalmente se ejecuta a través de una red o malla de proteínas que interactúan unas con otras y con otras moléculas relevantes dentro de las células.
Cuando todo el sistema es visto como una red o malla de eventos interrelacionados, la enfermedad puede considerarse como una consecuencia de que algo ha perturbado la información patrón del programa de la red-malla.
 |
| Gráfico14 |
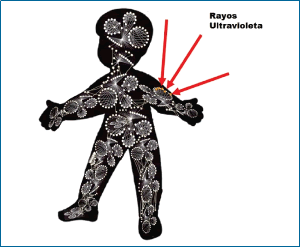
La causa inicial podría ser una falla dentro del sistema tal como un cambio casual en el ADN, que altera el código de instrucciones, o un efecto del medio ambiente, como por ejemplo los rayos ultravioleta de la luz solar que son capaces de desencadenar cambios en el ADN (Gráfico 15). Como una disrupción inicial produce efectos secundarios inmediatos y estos se retroalimentan y los patrones de información continúan replicándose, estos patrones de cambios explican el proceso de la enfermedad como una secuencia mecánica.
 |
| Gráfico 15 |
Como todas las sustancias producidas por las células se vierten en la sangre, el grupo de California se ha propuesto usar el dosaje en sangre para evaluar el status de todo el sistema de red-malla interconectado corporal (SRMIC) comparando las poblaciones de ARN mensajero producidas en los 50 órganos y tejidos del individuo (DADO QUE LA SANGRE BAÑA TODOS LOS ORGANOS, CONSTITUYE UNA EXCELENTE VENTANA PARA ESTUDIAR TODO EL SISTEMA ORGÁNICO. NIVELES ANORMALES DE UNA PROTEÍNA DADA PUEDE SER UNA SEÑAL DE ALTERACIÓN DE UN ÓRGANO ESPECÍFICO) (Gráfico 16).
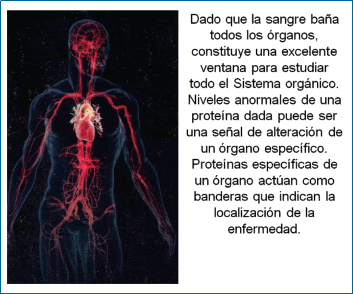 |
Gráfico 16
|
Los investigadores han encontrado que en cada órgano hay alrededor de 50 ARNs que son primariamente producidos en ese órgano (11). Algunos de ellos codifican proteínas específicas para el órgano. Cuando hay una perturbación en el sistema esa proteína se eleva o disminuye en la sangre lo cual puede ser una señal específica “del órgano” en donde está el disturbio (LAS PROTEÍNAS ESPECÍFICAS DE UN ÓRGANO ACTÚAN COMO BANDERAS QUE INDICAN LA LOCALIZACIÓN DE LA ENFERMEDAD).
Si, por ejemplo, de las 50 proteínas específicas existentes en cada órgano, pudieran ser mesuradas la mitad (lo cual significaría la posibilidad de hacer 1250 análisis simultáneos), a través de un análisis computacional, sería posible detectar qué red-malla está perturbada, simplemente por su medición en la sangre. Y así reconocer un órgano que comienza a mostrar un cambio que conduce a la enfermedad.
Más allá que detectar tempranamente el inicio de una disrupción –que es tan importante por ejemplo en el cáncer-, esta metodología nos daría la capacidad de estratificar la alteración de un sujeto en relación con sus variantes, sus tipos o estadios, seguir su progreso y evaluar la respuesta si intentamos alguna forma de corrección. Davis y col. de la Escuela de Medicina de Emory, (Atl.Georgia), han iniciado la demostración de la validez de esta tesis siguiendo la evolución de la enfermedad prión en pericotes. Para ello inyectaron a pericotes con proteínas prion infectante que conduce a un proceso degenerativo cerebral del tipo de la llamada “enfermedad de las vacas locas” o la enfermedad de Creutzfeldt-Jakob en el hombre, luego analizaron la totalidad de los ARN mensajeros que corresponden al cerebro en los animales infectados y en controles en 10 diferentes momentos del proceso. De estos datos, los investigadores identificaron 300 cambios de ARN que comprendían la esencia que certificaba la respuesta a la enfermedad de prion. Cerca de 200 de esos ARN pertenecían a 4 red-mallas que explicaban todos los aspectos de la enfermedad. Este estudio permitió también identificar 4 proteínas de la sangre que predecían la enfermedad antes que ella fuera sintomática, obvio valor para la medicina preventiva. Estos estudios requirieron alrededor de 30 millones de mediciones y necesitaron la implementación de un software especial para analizar, integrar y modelar esta enormidad de datos, pero han demostrado que el sistema de Red Malla Orgánica Interconectado, propuesto, es válido (11).
El gráfico 17 ejemplifica una ocurrencia reconocida recientemente en el hombre, para la próstata, por el profesor J.R. Heath del Biosystems Biology Cancer Center. Puede verse cómo la proteína MAPK8, reguladora del movimiento celular, se eleva en el estado inicial del proceso y cómo los niveles de la proteína CDC1 se hacen 16 veces mayores en la fase tardía del cáncer prostático (11). Esto es un ejemplo, en el hombre, de cómo dos proteínas nos dan indicio de la presencia y progreso de la enfermedad.
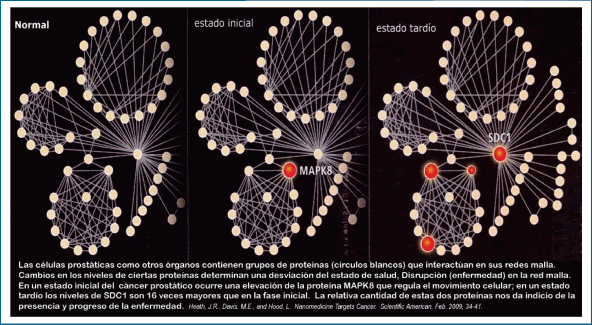 |
Gráfico 17
|
Construir estos modelos de red-malla predictivos y hacerlos viables y útiles para el trabajo médico hacen necesario contar con técnicas rápidas, sensitivas y sobretodo baratas para secuenciar el ADN, medir el ARN y las proteínas resultantes. Este desarrollo de técnicas está en pleno proceso.
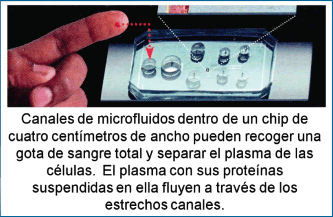 |
Gráfico 18
|
Heath & Hood del Instituto Tecnológico de California, han desarrollado un chip de 4 cm. de ancho que mide niveles de proteína en una gota de sangre usando una variante miniaturizada de una estrategia de detección convencional (Gráfico 18).
El chip está hecho de vidrio plástico y reactivos, de tal manera que es barato de producir (Gráfico 19). El dispositivo toma alrededor de 2 milímetros cúbicos de sangre, separa las células del plasma y mide, utilizando reactivos inmunológicos y marcación fluorescente, alrededor de una docena de proteínas que luego se exhiben en un código de barras (Gráfico 20); todo esto en un período de unos pocos minutos desde la colección de sangre (11). El costo calculado de esta versión prototipo es de 5 a 10 centavos de dólar por cada proteína analizada. Se espera que cuando esta versión esté totalmente desarrollada (capaz de hacer, no una docena, sino cientos de análisis simultáneos) estará en condiciones de cubrir la demanda de la Red-Malla Orgánica Individual que requiere el modelo de medicina temprana o “Early Health Model”.
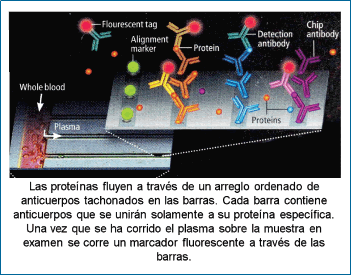 |
| Gráfico 19 |
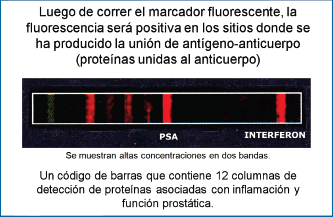 |
| Gráfico 20 |
Ampliar la capacidad de los chips para medir cientos o miles de proteínas tomará algún tiempo, pero los avances en los diseños de microfluidos químicos de superficies y en la ciencia de mediciones están reduciendo rápidamente la brecha entre lo que es posible hoy y lo que se requerirá para hacer una medicina totalmente personalizada y dentro del concepto de “The Early Health Model” o Salud Temprana.
Estamos, pues, frente al inminente logro de un conocimiento PREDICTIVO de la enfermedad.
Sobre el Sistema de enfermedad
Siguiendo esta línea de raciocinio, el desarrollo de un llamado SISTEMA DE ENFERMEDAD, implica concebir que un análisis de la Red Malla Orgánica permitirá descubrir el punto inicial y la vía y canales de perturbación. Se trata de un enfoque individual o personalizado en la medicina temprana. Y subraya también que, conocedores de las vías perturbadas, o en camino de perturbarse, podremos actuar, tratando de corregir estas desviaciones, con medidas y terapéuticas que serían entonces parte de una NUEVA MEDICINA PREVEN- TIVA.
En este intento de actuar a nivel de las vías perturbadas, de la malla orgánica, la nanotecnología está llamada a cumplir una importante función. De aquí que debamos decir algunas palabras sobre la Nanotecnología en Medicina.
La Nanotecnología
A la escala de nanómetros (mil millonésima de un metro) sustancias químicas y dispositivos pueden interactuar con las células y moléculas biológicas de una manera singular (Gráfico 21). La figura da una idea de la dimensión comparativa de compuestos y dispositivos con elementos conocidos. Las Nanotecnologías usadas en investigaciones y en terapias son del rango de 10 nanómetros –proteína o anticuerpo- y de 100 nm el tamaño de un virus.
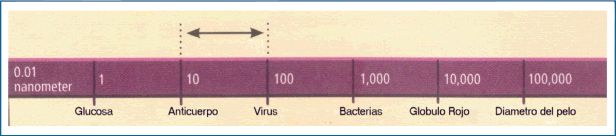 |
| Gráfico21 |
Estas partículas o dispositivos se aplican como sensores para detectar moléculas, como proteínas o ADN, como mejoradores de imágenes y como medios para dirigir, con especificidad al tejido blanco deseado, el agente terapéutico. Se pueden construir partículas compuestas de varios materiales que contienen en su corazón moléculas terapéuticas para ser liberadas en el momento y en el lugar que deseemos. Tales vehículos de envío dirigido pueden ser hechos de simples cápsulas lipídicas que filtran pasivamente a través de las paredes de los vasos en el tejido enfermo, permitiendo el pasaje de las drogas ordinarias. Las nanopartículas con diseño más complejo pueden incluir en su capa externa anticuerpos que actúan como proteínas de transferencia por ser específicas, por ejemplo, para un tumor dado (Gráfico 22). El gráfico 23 nos muestra el efecto de nanocristales encapsulados en látex que responden a la luz emitiendo fluorescencia. Anticuerpos adheridos a su superficie hacen que se fijen en el tumor que queremos revelar por los sistemas de imágenes convencionales.
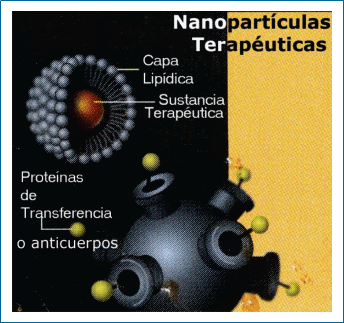 |
| Gráfico 22 |
Trabajar con nanopartículas nos da una gran ventaja de manejo, ellas pueden ser ensambladas con una variedad de drogas quimioterapéuticas o con filamentos de ADN silenciadores de genes (12). Estos ensambles o cargas de encapsulamiento de los “nanodispositivos” pueden ser no solo lipídicos sino también de distintas sustancias como polímeros o minerales, y si están recubiertos de anticuerpos específicos, como hemos ilustrado, para ciertas moléculas, los podemos direccionar a nuestros objetivos o tejidos blanco. Esta modalidad nos da una gran flexibilidad para actuar en el lugar que deseemos o en el momento que requerimos.
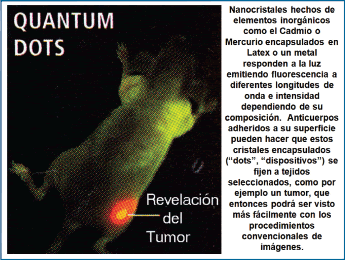 |
| Gráfico 23 |
Como vemos existen, en desarrollo, caminos para poder actuar a nivel de las vías o canales perturbados de la Red Malla Orgánica.
Esta concepción del Sistema Biológico aplicado a la enfermedad, está llevando al desarrollo de nuevas tecnologías que comprenden no solo el análisis de microfluidos y nanotecnología sino nuevos instrumentos de medición y visualización y nuevas modalidades de computación que pueden analizar, integrar y hacer modelos de gran cantidad de información biológica (13).
En los siguientes 10 a 20 años la medicina predictiva y la medicina personalizada serán materia de una revolución por lo menos en dos aspectos:
1. La secuencia de cada genoma individual, permitirá con creciente seguridad conocer el probable futuro de salud de cada individuo.
2. La medición cada vez menos cara, de proteínas sanguíneas nos permitirá evaluar, regularmente y comprensivamente, cómo está evolucionando la salud de cada individuo.
La medicina preventiva comienza con la detección de alguna disrupción ya manifiesta en la Red Malla Orgánica, a través de una proteína fuera de nivel, lo que nos da la oportunidad de intentar restaurar la Red Malla Orgánica a la normalidad y, eventualmente, el desarrollo de drogas profilácticas.
El Nuevo Modelo de Medicina
Se calcula que en las siguientes dos décadas la Medicina cambiará de su modelo actual, en el que los médicos esperan que la gente se ponga enferma, a un modelo que es, de lejos, más racional en el que los doctores buscarán las perturbaciones que pueden conducir, en el futuro, al desarrollo de enfermedades. Lo que está produciendo este cambio o nuevo modelo de Sistema Médico son las nuevas tecnologías de medición.
Mientras que en el pasado se estudiaba la enfermedad analizando los efectos de un gen en cada prueba, el nuevo Sistema le dará la habilidad de analizar todos sus genes a la vez.
El promedio de visitas hoy al consultorio médico implica examinar la presión arterial, la temperatura, los exámenes de sangre y otras determinaciones rutinarias. En el futuro cercano los médicos coleccionarán billones de bytes de información acerca de cada individuo: GENES, PROTEÍNAS SANGUÍNEAS, CÉLULAS Y DATOS HISTÓRICOS. Ellos utilizarán esta “data” para reconocer si la información biológica de sus células en la red malla y circuitos ha sido perturbada, sea por defectos del gen o por exposición a factores negativos del ambiente o por ambos. Nuevas computadoras almacenarán gran cantidad de datos obtenidos anualmente de cada individuo y los convertirán en una fuente de información acerca de las condiciones de salud y enfermedad.
Los doctores serán capaces de secuenciar el genoma de cada paciente, y en conjunto con todos los datos podrán hacer una útil predicción acerca del futuro de la salud de ella o de él. Serán capaces de decirle, por ejemplo, tú tienes el 30% de riesgo de desarrollar un cáncer de ovario antes de los 30 años (Medicina Predictiva). Un estudio bianual de su sangre hará posible obtener información sobre el actual estado de salud de cada uno de los 50 órganos de su sistema. Estos pasos colocarán el foco de la Medicina en el paciente individual (Medicina Personalizada).
La aplicación de esta medicina sistemática servirá para desarrollar drogas que ayuden a prevenir enfermedades. Si, por ejemplo, uno tiene el 50% de la chance de desarrollar un carcinoma de próstata para la edad de 50 años, será posible comenzar a tomar drogas cuando tiene 30 años, lo que reducirá sustancialmente la probabilidad señalada (Nueva Medicina Preventiva). El foco del cuidado de la salud se moverá de tratar enfermedades a mantener las condiciones de salud.
La Medicina Participativa significa la oportunidad que nunca han tenido los pacientes de tomar el control de su propia salud. Esto es, el individuo que estará al tanto de sus niveles proteicos en cada una de las redes de su malla interco-nectada podrá, al sorprender alguna desviación, alertar al médico que lo controla señalándole la ocurrencia de esta desviación, y el médico estará en condiciones de poder intentar corregir esta inicial perturbación. En esta forma el paciente estará participando en el propio control de su salud.
Nuevas compañías que pueden analizar las variaciones del genoma humano como “23andme” (Mountain View, California) y “Navigenics” (Foster City, California) están ya planeando proveer a los pacientes con información genética que puede ser útil para modificar su comportamiento y evitar problemas potenciales. En octubre del 2008, el “Scripps Translational Science Institute” asociado con las compañías Navigenics, Microsoft Corporation y Affymetrix anunció el inicio de un estudio que durará 20 años, denominado “Scripps Genomic Health initiative” en donde se estudiarán miles de individuos en los que, después de haber realizado las pruebas genéticas, se harán las indicaciones pertinentes para intentar modificar las vías perturbadas que el estudio defina. En julio del 2009 Navigenics redujo el precio del estudio genético básico, que antes costaba miles de dólares, a $999.
Así como ahora, sabemos que el fumar a menudo causa cáncer pulmonar o que la exposición a la luz solar causa cáncer de piel, en el futuro los pacientes necesitarán no solamente datos genéticos sino también conocimientos sobre factores del medio ambiente capaces de activar o desactivar genes y causar enfermedades.
 |
Gráfico 24
|
A este nuevo enfoque en el manejo del acto médico el Dr. Leroy Hood, del Instituto Tecnológico de California, le ha denominado MODELO DE MEDICINA P4 (14) (Gráfico 24).
Obviamente, ello va a introducir nuevas variables en la relación médico-paciente, en la industria farmacéutica, en la industria alimentaria y en las compañías de seguros. Hoy los clínicos no están preparados ni entrenados para esto. Las compañías de seguros tampoco; los seguros de Salud solo reconocen beneficios para el enfermo con diagnóstico probado. Las compañías farmacéuticas descansan en los derechos de propiedad intelectual de drogas que han demostrado efectividad en enfermedades ya establecidas y comprobadas.
La investigación también tendrá que cambiar. La mayor parte de las enfermedades importantes como diabetes, cáncer, enfermedades cardíacas, obesidad y Alzheimer, son tan complejas que los acercamientos que hasta ahora hemos tenido de ellas, para estudiarlas, solo han mostrado resultados marginales. Con el nuevo enfoque habrán de desarrollarse nuevos sistemas de exploración de estos procesos.
La educación médica también tendrá que transformar-se, si bien hoy, como ya lo hemos dicho, estamos haciendo uso puntual de muchas de las novedades de las nuevas tecnologías, la clasificación que hacemos de las enfermedades se basa en unos pocos parámetros mesurables. En el futuro, los médicos necesitarán familiarizarse con la complejidad de los sistemas biológicos humanos y tendrán que trabajar de la mano con una serie de armas basadas en la computación. Los médicos se enfrentarán a pacientes que tienen una enorme cantidad de información a su disposición. Los más optimistas piensan que en el futuro los doctores, más que tener que preocuparse de la enfermedad, estarán embarcados en cómo mantener la condición de bienestar. Mi experiencia me indica que estas auspiciosas previsiones debemos tomarlas con cautela y no al pie de la letra.
De otro lado, y finalmente, la digitación de la medicina -que es nuestra habilidad de extraer y almacenar información relevante sobre el ADN y las moléculas activas en la sangre de cada individuo- conjuntamente con los cambios revolucionarios en el diagnóstico, terapéutica y prevención; permitirían, de lograrse, como se pretende, la disminución del costo de las pruebas más sofisticadas, llevar la nueva medicina a los sectores menos favorecidos. Esto haría posible que, por fin, se cumpla con la Declaración Universal de los Derechos del Hombre, que establece que toda persona tiene derecho a un nivel de vida adecuado que le asegure la salud y el bienestar. El lema: “Salud para todos en el Mundo”, hasta hoy inalcanzable, sería recién, entonces, ¡una realidad! ¡Hagamos votos para que así sea!
Referencias Bibliográficas
- Mellors RC. Analytical Cytology. 2nd. Edition. Mc. Graw-Hill Book Company. 1959.
- Weinstein, RS. The S-Curve Framework. Predicting the Future of Anatomic Pathology. Arch. Pathol. Lab. Med. 2008;132:739-742.
- O’Malley D. Practical Applications of Telepathology using Morphology-Based anatomic Pathology. Arch. Pathol. Lab. Med. 2008;132:743-747.
- Kass, ME. The future escape of Pathology. Conference. Introduction. Arch. Pathol. Lab. Med. 2008;132:733.
- Schwartz JN.The future escape of Pathology. Conference. Overview. Arch. Pathol. Lab. Med. 2008;132:734.
- Lewin B. Genes VII. Oxford University Press, 2000.
- Watson JD, Crick FHC. Molecular Structure of Nucleic Acids. A Structure for Desoxyribose Nucleic Acid. Nature. 1953;171: 737.
- Ross DW. Introduction to Molecular Medicine, Second Edition, Springer. New York 1996.
- Majno G, Joris I. Cells, Tissues and disease. Principles of General Pathology. Blackwell Science, Cambridge, Massachusetts 1996.
- Friedman BA.A survey of the Myriad Forces Changing Anatomic Pathology and their consequences. Arch. Pathol. Lab. Med. 2008;132:735-738.
- Heath JR, Davis ME, Hood L. Nanomedicine Targets Cancer. Scientific American, 2009;34-41.
- Davis ME, Zuckerman JE, Choi Chung H, Seligson D, Tolcher A, Alabi CA, Yen Y, Heidel JD, Ribas A. Evidence of RNAi in humans from systemically administered siRNA via targeted nanoparticles. Nature 2010;464:1067-1071.
- Arias-Stella J. El Futuro de la Patología. Diagnóstico: 2009; 48(1):23-32.
- Hood L. A doctor’s Vision of the future of Medicine. Institute for System Biology in Seattle, Washington. Newsweek, 2009;6:13.
1 Profesor Emérito. Universidad Peruana Cayetano Heredia. Fellow Royal College of Pathologists.
* Presentado en clase del Recuerdo “Promoción Médica San Fernando 1960", 7 Oct. 2010; y,
Clase magistral,“Promoción Oswaldo Hercelles 1955", Bodas de Esmeralda, 28 Oct. 2010. |
