Los retos actuales en el tratamiento de la diabetes mellitus tipo 2
Desde el año 1921, en el que Banting y Best descubrieron la insulina y su posterior introducción en el tratamiento de la diabetes mellitus, se han efectuado avances muy importantes en la terapia de esta enfermedad con la incorporación de las sulfonilureas, biguanidas, glitazonas, inhibidores de la a-glucosidasa, más recientemente los inhibidores de la dipeptidilpeptidasa 4 (DPP4) y los análogos de la glucagon-like peptide 1 (GLP1), y en fase experimental están los inhibidores de la reabsorción renal de la glucosa.
Pese a estos avances, que han permitido mejorar la expectativa y calidad de vida de los diabéticos, la terapia de la diabetes mellitus aún no ha alcanzado un nivel ideal y existen retos muy importantes como son el desarrollo de las manifestaciones crónicas, incremento de peso, hipoglicemia y la apoptosis de la células b del páncreas, que es necesario considerar para proporcionar una mejor atención a los pacientes que la padecen.
Con esta denominación nos referimos a las alteraciones producidas por las lesiones micro y macrovasculares, que consideramos inapropiado denominarlas complicaciones crónicas, como se señala en la literatura anglo sajona, desde que forman parte de la historia natural de la enfermedad.
Se conoce que ellas son el producto de 3 factores: la hiperglicemia sostenida, el tiempo de enfermedad y el factor genético que, en conjunto predisponen al diabético a desarrollar una microangiopatía responsable de alteraciones en el sistema nervioso (neuropatía diabética), ojos (oftalmopatía diabética), riñones (nefropatía diabética) y una macroangio-patía que lleva a alteraciones del aparato cardiovascular, causa del incremento de riesgo cardiovascular, expresado como eventos cardíacos, accidentes cerebrovasculares, alteraciones vasculares periféricas y formación de aneurismas ateroescleróticos.
Los estudios DCCT (1), UKPDS (2,3), Kumamoto (4) y muchos otros más han demostrado que el tratamiento, denominado intensivo, en el que se procura que la glicemia elevada se normalice, tuvieron un efecto muy favorable para disminuir la prevalencia de los eventos microvasculares.
En el estudio DCCT (1), realizado en diabéticos tipo 1 se consiguió una reducción de los eventos microvasculares, tanto en prevención primaria como secundaria como se muestra en la tabla 1.
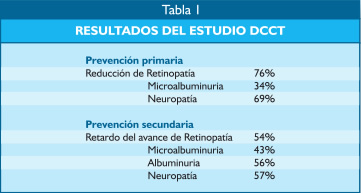
El estudio UKPDS (2,3) realizado en diabéticos de tipo 2, del mismo modo se obtuvo una disminución significativa de las alteraciones de origen microvascular con la terapia intensiva como se puede apreciar el la tabla 2.
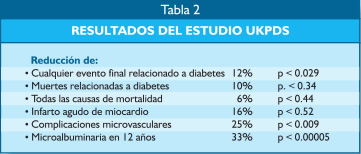
En el estudio Kumamoto (4), realizado así mismo en diabéticos tipo 2, la administración de insulina en forma intensiva permitió reducciones significativas de los eventos relacionados a la microangiopatía diabética.
En todos estos estudios, sin embargo, no se consiguió modificar las alteraciones macrovasculares; por el contrario, desde el antiguo estudio del denominado University Group Diabetes Program (5) publicado en 1970, ha estado en debate el tema sobre el efecto desfavorable de algunos hipoglicemiantes orales del grupo de las sulfonilureas y la fenformina sobre las alteraciones cardiovasculares. Schramm y col. (6) llevaron a cabo un estudio comparativo de 9 años sobre el efecto de los hipoglicemiantes insulino segretagogos y llegaron a la conclusión que la glimepirida, glibenclamida, glipizida y tolbutamida parecían estar asociadas a un mayor riesgo cardiovascular y mortalidad en comparación a la metformina, mientras que la repaglinida y gliclazida mostraron un menor riesgo.
Como se ha señalado anteriormente, se cuenta con nuevos medicamentos como los inhibidores de la a-glucosidasa, los inhibidores de la DPP4 y los análogos de la GLP1, que tienen mecanismos de acción diferentes y cuyos efectos sobre las manifestaciones crónicas está aún en estudio. A este respecto, recientemente Patil y col. han publicado los resultados de un meta análisis, en el que consignan que los inhibidores de la DPP4 mostraron un riesgo relativo (RR) para todo evento cardiovascular de 0.48 (0.31 to 0.75, p = 0.001) y de 0.40 (0.18 to 0.88, p = 0.02) para infarto miocárdico no fatal o para síndrome coronario agudo, que permite considerar que este grupo de hipoglicemiantes poseería un efecto beneficioso para disminuir la prevalencia de las manifestaciones crónicas relacionadas a la macroangiopatía diabética (7). En la actualidad se están corriendo estudios clínicos orientados específicamente a establecer si los inhibidores de la DPP4 y los agonistas de la GLP1 tienen algún efecto sobre las alteraciones macrovasculares como el TECOS, SAVOR-TIMI 53, CAROLINA. Para los análogos de GLP1, se evaluará linagliptina (estudio LEADER); exenatida (EXCEL); dulaglutida (REWIND); lixisenatida (ELIXA). Será necesario esperar dos o más años para conocer la influencia de este grupo de fármacos sobre la macroangiopatía diabética.
Control del peso corporal
Una de las metas importantes del tratamiento de la diabetes mellitus es el control del peso corporal. Como es bien conocido, la obesidad es uno de los factores mas reconocidos responsables del desarrollo de la diabetes de tipo 2, en particular por ocasionar resistencia a la insulina (8,9,10), en consecuencia es fundamental la prescripción del régimen alimenticio que proporcione al diabético estrictamente la cantidad de calorías necesarias para mantener un peso normal. De allí que resulte preocupante que algunos hipoglicemiantes tengan como efecto secundario el incremento de peso.
En la figura 1 se efectúa una comparación de los hipoglicemiantes de acuerdo a su efecto sobre el peso; se puede apreciar que las sulfonilureas, glinidas y glitazonas determinan incremento de peso de los pacientes, a los que se debe agregar la insulina; en cambio los inhibidores de la DPP4 no tienen efecto sobre el peso y mas bien los inhibidores de la a-glucosidasa, y los análogos de la GLP1 lo disminuyen (11).
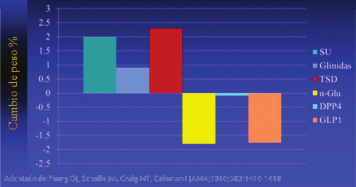
Hipoglicemia
La hipoglicemia es una complicación severa de la diabetes mellitus tanto de tipo 1 (DM1) como 2 (Dm2), tiene consecuencias graves sobre el sistema nervioso y cardiovascular, pudiendo llevar a la muerte en caso de no ser tratada a tiempo. En el diabético la hipoglicemia se puede presentar en forma espontánea, pero mucho más frecuentemente como consecuencia del tratamiento
La hipoglicemia espontánea se observa en el diabético obeso como una primera manifestación de la enfermedad y tiene las características de ser postprandial y tardía, es decir a la 4ta. ó 5ta. hora después de la ingesta de alimentos, debido a una gran hiperinsulinemia (Figura 2).

La hipoglicemia inducida se refiere a la producida por la administración hipoglicemiantes orales o insulina. Como se ha mencionado anteriormente, los estudios tanto DCCT como UKPDS han demostrado que los pacientes en tratamiento intensivo o sea cercano a un metabolismo intermediario normal tuvieron una disminución significativa del desarrollo de microangiopatía y así la aparición de nefropatía, oftalmopatía y neuropatía diabéticas; esto sin embargo se acompañó de un incremento de la tasa de episodios de hipoglicemia. En la figura 3 se grafíca el incremento de la tasa de episodios de hipoglicemia como producto de la terapia intensiva en diferentes estudios clínicos
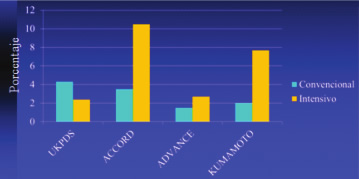
De acuerdo a la American Diabetes Association, la hipoglicemia ha sido clasificada de la siguiente forma:
• Hipoglicemia severa
• Hipoglicemia sintomática documentada
• Hipoglicemia asintomática
• Probable hipoglicemia sintomática
• Hipoglicemia relativa
En la producción de los episodios de hipoglicemia es importante considerar que existen situaciones que incrementan el riesgo a padecerlos, tales como:
1. Características farmacológicas del hipoglicemiante utilizado
2. Tipo de protocolo utilizado (convencional, intensivo)
3. Mala indicación del hipoglicemiante
4. Inadecuada ingestión de los alimentos
5. Compromiso de la función renal
6. Género femenino
7. Raza negra
8. Mala educación
9. Mayor edad
10. Duración prolongada de la enfermedad
11. Tratamiento con insulina
12. HbA1c basal alto
13. Individuos cuya HbA1c no cae rápidamente en los primeros 4 meses de tratamiento
En cuanto a las características farmacológicas del hipoglicemiante, la insulina es el medicamento que produce mayor número de episodios de hipoglicemia, le siguen las sulfonilureas y las glinidas, que tienen la particularidad de estimular la secreción pancreática de insulina y a través de este mecanismo poseen una mayor potencialidad para producir eventos de hipoglicemia que aquellos otros que actúan disminuyendo la resistencia a la insulina como la metfomina, inhibidores de la DPP4, análogos de la GLP1, inhibidores de la a-glucosidasa y las glitazonas.
Una inadecuada indicación de un hipoglicemiante, en particular a pacientes que inician la enfermedad puede llevar a la producción de hipoglicemia.
En pacientes que no llevan una apropiada alimentación, en especial referida a los horarios y la cantidad de alimentos de cada colación puede ser la causa de episodios de hipoglicemia.
Los diabéticos con insuficiencia renal son más pro- pensos a presentar situaciones de hipoglicemia, por lo que requieren un cuidado especial, en el que se debe efectuar una adecuada elección del hipoglicemiante y de la dosis del mismo.
En la tabla 3 se describen los daños que la hipoglicemia produce, en particular sobre el sistema nervioso y el aparato cardiovascular (12-18).

Apoptosis de las células b del páncreas
Uno de los problemas centrales y en debate de la diabetes mellitus es la apoptosis de las células beta del páncreas que, en tiempo variable, lleva a que los pacientes diabéticos deban recibir insulina como único tratamiento viable.
Se debe recordar que el páncreas posee alrededor de un millón de islotes de Langerhans y que cada uno de ellos contiene ~1,000 células endocrinas, 75% de las cuales son células beta, encargadas de producir insulina a partir de la proinsulina. La masa de células beta se mantiene por un proceso de replicación mas que por una derivación de las células madre, proceso que está vinculado a la concentración de la glucosa, cuando esta se incrementa se produce un incremento de la replicación de células beta. Las células beta son excitables eléctricamente de tal modo que los cambios de los potenciales de la membrana celular ocasionados por los cambios de la concentración de glucosa determinan las variaciones de la secreción de insulina (25).
El inicio de la DM2 está marcado por un incremento de la resistencia a la insulina a nivel de los tejidos periféricos que provoca una secreción incrementada de esta hormona hiper-insulinismo). Al persistir esta situación progresivamente se observa una declinación de la secreción de insulina que en gran magnitud, es de carácter funcional y, posteriormente, por disminución relativa de la masa de células beta, es decir que en el paciente diabético con hiperglicemia se produce una deficiencia en la replicación de las células beta, proceso de apoptosis cuyo mecanismo íntimo de producción no se conoce bien y menos la forma de evitar o frenarlo (26). En los últimos años, sin embargo, ha aparecido información que permite atisbar la posibilidad de modificar este proceso; así Song y col. han encontrado que la administración de Exetidina a ratones estimula la proliferación de células beta (27). Faradji y col. (28), en un número pequeño de pacientes diabéticos que recibieron transplantes de células beta, pudieron observar que la adición de Exetidina en el protocolo de mantenimiento de los transplantes permitió una sobrevivencia mayor de los mismos que la de los que no recibieron este análogo de la GLP1.
Xu y col. (29) recientemente han llamado la atención sobre la existencia de la thioredoxin-interacting protein (TXNIP), cuya expresión en exceso facilita la apoptosis de las células beta. Esta proteína se activa en presencia de la glucosa y está incrementada en animales diabéticos, lo que podría constituir la primera explicación del efecto «tóxico» de la glucosa. Estos autores, en experimentos in vitro con cultivos de células beta de ratas y de humanos, encontraron que la administración de Verapamil, un bloqueador de los canales de calcio, promovió la sobrevivencia de las células b; del mismo modo, en experimentos in vivo con ratones obesos ob/ob y en ratones hechos diabéticos por la administración de estreptozotocina, el Verapamil previno la aparición de la diabetes experimental, experiencias que abren nuevas vías de investigación en relación a la apoptosis de las células beta del páncreas.
Conclusiones
Desde el descubrimiento de la insulina (1921) y la introducción de agentes orales en monoterapia o en combinaciones, con mecanismos de acción diferentes, se ha mejorado el control metabólico y las condiciones de vida de los pacientes diabéticos, con disminución significativa de la morbimortalidad por complicaciones agudas y el desarrollo de manifestaciones crónicas.
Las manifestaciones crónicas, incremento de peso, hipoglicemia y la apoptosis de las células b son actualmente los principales retos de la terapia de los pacientes diabéticos tipo 2.
La hiperglicemia, tiempo de enfermedad e influencia genética son las principales causas de las manifestaciones crónicas
El tratamiento intensivo es eficaz para disminuir significativamente el desarrollo de las manifestaciones crónicas microvasculares tanto en prevención primaria como secundaria, sin embargo, se ha observado un incremento de la tasa de episodios de hipoglicemia.
Existen evidencias que demuestran que los inhibidores de la DPP4 disminuyen la incidencia de las manifestaciones crónicas macrovasculares.
Existen indicios experimentales que los análogos de la GLP1 así como los bloqueadores de los canales de calcio disminuyen la apoptosis de las células b del páncreas.
Recomendaciones
Se debe diagnosticar la diabetes en sus estadíos más tempranos e iniciar su tratamiento.
El tratamiento debe ser individualizado, tomando en consideración no solo al trastorno metabólico sino también a las morbilidades conexas como la hipertensión arterial y la dislipoproteinemia.
Se debe iniciar el tratamiento de los pacientes prescribiendo un cambio del estilo de vida mediante un régimen alimenticio de acuerdo estrictamente a las necesidades calóricas de cada paciente, actividad física y un programa de educación al paciente y su familia.
Cuando estas primeras medidas no sean suficientes, se debe recurrir a la administración de un hipoglicemiante oral, metformina y/o un inhibidor de la DPP4.
En esta enfermedad crónica, el seguimiento debe ser periódico, en lapsos no mayores de 3 meses, para mantener un adecuado control clínico y metabólico (HbA1c < 7%), que evite el desarrollo de manifestaciones crónicas, incremento de peso, episodios de hipoglicemia y retarde la apoptosis de las células béta y una adecuada sobrevivencia (30).

